NOYAUX-MASSE ET ÉNERGIE
1.1 Relation d'Einstein
Albert Einstein avait montré que tout système de masse $m$, au repos, possède une énergie due à sa masse, appelée énergie de masse qui s'écrit :
- $E$ : énergie du système (J).
- $m$ : masse du système (kg).
- $c$ : célérité de la lumière dans le vide ($c \simeq 3 \cdot 10^8$ m.s$^{-1}$).
Application 1
Calculer l'énergie de masse d'un proton ($m_p = 1,6726 \cdot 10^{-27}$ kg).
Réponse :
$E = m_p \cdot c^2 = 1,6726 \cdot 10^{-27} \cdot (3 \cdot 10^8)^2 = 1,505 \cdot 10^{-10}$ J
Remarque
Lorsque la masse du système varie de $\Delta m$, l'énergie masse du système varie de $\Delta E = \Delta m \cdot c^2$.
- Lorsque la masse du système diminue $\Delta m < 0$ donc $\Delta E < 0$. Le système fournie de l'énergie au milieu extérieur.
- Lorsque la masse du système augmente $\Delta m > 0$ donc $\Delta E > 0$. Le système reçoit de l'énergie au milieu extérieur.
1.2 Unités de masse et d'énergie
♠ Unité de la masse adaptée en physique nucléaire est l'unité de masse atomique de symbole $u$ telle que : $1u = 1,66 \cdot 10^{-27}$ kg
$1u$ vaut $\frac{1}{12}$ de la masse d'un atome de Carbone 12 : $1u = \frac{1}{12} \cdot \frac{M(^{12}_6 C)}{N_A} = \frac{1}{12} \cdot \frac{12 \cdot 10^{-3}}{6,02 \cdot 10^{23}} = 1,66 \cdot 10^{-27}$ kg
♠ Unité de l'énergie adaptée en physique nucléaire est l'électronVolt de symbole eV telle que : $1$ eV $= 1,6 \cdot 10^{-19}$ J
L'unité la plus utilisée est Méga électron-Volt (MeV) telle que : $1$ MeV $= 10^6$ eV $= 1,6 \cdot 10^{-13}$ J
♠ Énergie équivalente à l'unité de masse atomique $u$ : On a : $E = m \cdot c^2 = 1,660054 \cdot 10^{-27} \cdot (299792458)^2$
$E = 1,49242 \cdot 10^{-10}$ J $= \frac{1,49242 \cdot 10^{-10}}{1,602177 \cdot 10^{-13}} = 931,5$ MeV
C'est à dire : $1u \cdot c^2 = 931,5$ MeV, donc : $1u = 931,5$ MeV.$c^{-2}$
2.1 Défaut de masse
- La masse du noyau est inférieure à la somme de masses des nucléons qui constituent ce noyau.
- Le défaut de masse $\Delta m$ d'un noyau $^A_Z X$ est la différence entre la somme de masses des nucléons et la masse du noyau :
avec $m_p$ : masse du proton, $m_n$ : masse du neutron, $m(^A_Z X)$ : masse du noyau
Remarque
Le défaut de masse est une grandeur positive : $\Delta m > 0$.
Application 2
Calculer, en (u) et en (kg), le défaut de masse du noyau du carbone $^{14}_6 C$.
On donne : $m_p = 1,00728$ u, $m_n = 1,00866$ u, $m(^{14}_6 C) = 13,9999$ u, $1u = 1,66 \cdot 10^{-27}$ kg
Réponse :
$\Delta m = [6 \cdot m_p + (14 - 6) \cdot m_n] - m(^{14}_6 C) = [6 \times 1,00728$ u $+ 8 \times 1,00866$ u$] - 13,9999$ u $\Rightarrow \Delta m = 0,11306$ u
$\Delta m = 0,11306 \times 1,66 \cdot 10^{-27} = 1,8768 \cdot 10^{-28}$ kg
2.2 Énergie de liaison
L'énergie de liaison $E_{\ell}$ d'un noyau est l'énergie qu'il faut fournir à ce noyau, au repos, pour séparer ses nucléons tels que ces nucléons soient également au repos :
avec : $\Delta m$ : défaut de masse et $c$ : célérité de la lumière dans le vide.
Application 3
Calculer, en MeV et en J, l'énergie de liaison du noyau de carbone $^{14}_6 C$ utilisé dans l'application 2.
Réponse :
- en MeV : $E_{\ell} = \Delta m \cdot c^2 = 0,11306$ u $\times c^2 = 0,11306 \times 931,5$ MeV.$c^{-2} \times c^2 = 105,3154$ MeV
- en J : $E_{\ell} = \Delta m \cdot c^2 = 1,8768 \cdot 10^{-28} \times (3 \cdot 10^8)^2 = 1,68912 \cdot 10^{-11}$ J
2.3 Énergie de liaison par nucléon
On exprime l'énergie de liaison d'un nucléon $\xi$ par la relation :
avec : $E_{\ell}$ : énergie de liaison et $A$ : nombre de nucléons du noyau.
L'unité de $\xi$ est : MeV/nucléon
Remarque : Plus l'énergie de liaison par nucléon est importante, plus le noyau correspondant est stable
Application 4
Calculer l'énergie de liaison par nucléon du noyau de carbone $^{14}_6 C$ utilisé dans l'application 3.
Réponse
$\xi(^{14}_6 C) = \frac{E_{\ell}(^{14}_6 C)}{A} = \frac{105,3154}{14} = 7,5225$ MeV/nucléon
2.4 Courbe d'Aston
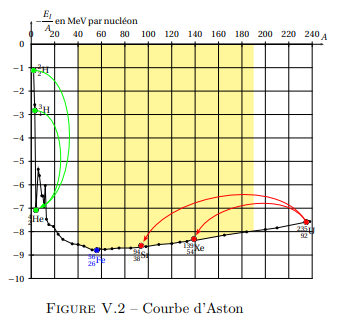
⋆ La courbe d'Aston donne l'évolution de l'opposé de l'énergie de liaison par nucléon $-\xi$ en fonction de nombre de nucléons $A$ du noyau. Il met en évidence la possibilité de transformation des noyaux en autres.
- Pour $20 < A < 190$, on constate que $-\xi$ prend des valeurs minimales qui correspondent aux noyaux plus stable.
- Pour $A < 20$, on constante que $-\xi$ augmente rapidement. il correspond aux petits noyaux instables ce qui pousse ces noyaux à s'associer entre eux pour former d'autres noyaux plus lourds plus stables. Ce phénomène est appelé Fusion nucléaire.
- Pour $A > 190$, on constate que $-\xi$ augmente lentement. Les noyaux correspondants sont instables ce qui leur poussent à se dissocier pour former d'autres noyaux plus légers plus stable. Ce phénomène est appelé Fission nucléaire.
3.1 Fission nucléaire
La fission nucléaire est une réaction nucléaire induite ou provoquée, au cours de laquelle un noyau fissile (Lourd) est bombardé (collision) par un neutron thermique, pour donner deux noyaux plus légers.
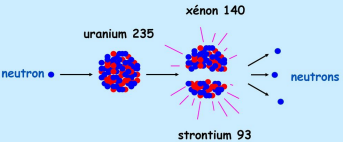
Exemples :
- $^{235}_{92} U + ^1_0 n \rightarrow ^{94}_{38} Sr + ^{140}_{54} Xe + 2^1_0 n$
- $^{235}_{92} U + ^1_0 n \rightarrow ^{140}_{35} Cs + ^{93}_{37} Rb + 3^1_0 n$
Remarques :
- La fission nucléaire est une réaction en chaîne. Elle produit des neutrons qui peuvent provoquer d'autre réactions de fission. Pour l'arrêter il faut ralentir les neutrons par des modérateurs comme l'eau et le graphite.
- La réaction en chaîne doit être contrôler pour qu'elle ne soit pas explosive (le cas de la bombe A - Bombe atomique). lorsque la fission est contrôlée. c'est le cas des réacteurs nucléaires où l'énergie est convertie en énergie électrique.
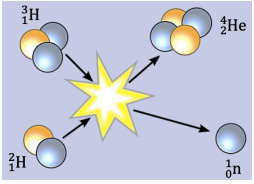
3.2 Fusion nucléaire
La fusion nucléaire est une réaction nucléaire provoquée, au cours de laquelle deux noyaux légers s'associent pour former un noyau plus lourd et plus stable.
Ces types de réactions se produisent dans le soleil et les étoiles où ils se forment des noyaux d'hélium.
Exemple :
- $^2_1 H + ^3_1 H \rightarrow ^4_2 He + ^1_0 n$
- $^1_1 H + ^2_1 H \rightarrow ^3_2 He$
- $^8_4 Be + ^4_2 He \rightarrow ^{12}_6 C$
Remarques :
- La fusion de deux noyaux ne se produit que si l'énergie cinétique des noyaux est suffisante pour échapper aux interactions répulsives.
- La fusion nucléaire est accompagnée d'une énergie dégagée qui est énorme. C'est le principe de la bombe H (Bombe Hydrogène).
On considère la réaction nucléaire modélisée par l'équation suivante :
$^{A_1}_{Z_1} X_1 + ^{A_2}_{Z_2} X_2 \rightarrow ^{A_3}_{Z_3} X_3 + ^{A_4}_{Z_4} X_4$
⋆ Le bilan massique $\Delta m$ (ou variation de masse) est : $\Delta m = [m_{\text{produits}} - m_{\text{réactifs}}]$ c'est à dire :
⋆ Le bilan énergétique (ou énergie de réaction) est : $\Delta E = E_f - E_i = m_f \cdot c^2 - m_i \cdot c^2 = (m_f - m_i) \cdot c^2 = \Delta m \cdot c^2$
C'est à dire :
Remarques :
- $\Delta E < 0$ : la réaction est exothermique (dégage de l'énergie).
- $\Delta E > 0$ : la réaction est endothermique (reçoit de l'énergie).
- L'énergie libérée par une réaction est : $E_{\text{libérée}} = |\Delta E|$
- On peut calculer l'énergie de la réaction à partir des énergies de liaisons $E_{\ell}$ :
Diagramme énergétique d'une réaction nucléaire.
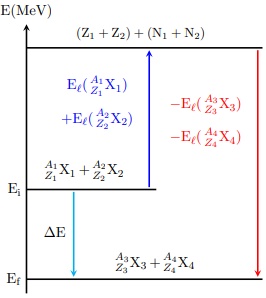
- $E_i$ : énergie initiale du système.
- $E_f$ : énergie finale du système.
- $E(X_1) + E(X_2)$ : énergie reçue par le système pour séparer les deux noyaux $X_1$ et $X_2$.
- $-E_{\ell}(X_3) - E_{\ell}(X_4)$ : énergie libérée par le système lors de la formation des noyaux $X_3$ et $X_4$ à partir des nucléides $Z_1 + Z_2$ et $N_1 + N_2$.
- $\Delta E < 0$ : L'énergie de la réaction est l'énergie libérée par le système pour qu'il soit plus stable : $E_{\text{libérée}} = |\Delta E|$
Application
Calculer l'énergie libérée de la réaction de fusion suivante : $^2_1 H + ^3_1 H \rightarrow ^4_2 He + ^1_0 n$
On donne : $m(^2_1 H) = 2,0136$ u, $m(^3_1 H) = 3,0155$ u, $m(^4_2 He) = 4,0015$ u, $m(^1_0 n) = 1,0087$ u
On rappelle que : $1u = 931,5$ MeV.$c^{-2}$
Réponse
$\Delta E = \Delta m \cdot c^2 = [m(^4_2 He) + m(^1_0 n) - m(^2_1 H) - m(^3_1 H)] \cdot c^2$
$\Delta E = [4,0015 + 1,0087 - 2,0136 - 3,0155] \times 931,5$ MeV.$c^{-2} \cdot c^2 = -0,0189 \times 931,5 = -17,605$ MeV
$E_{\text{libérée}} = |\Delta E| = 17,605$ MeV
5.1 Effets biologiques de la radioactivité
Tous les être-vivants sont exposés à une quantité de rayonnement, leurs effets dépendent de l'intensité du rayonnement ainsi que son type.
- Rayonnement $\alpha$ : peut causer des brulures au niveau de la peau.
- Rayonnement $\beta$ : il est utilisé pour le traitement des cancers.
- Rayonnement $\gamma$ : il est utilisé dans le diagnostique des maladies par imagerie.
5.2 Applications de la radioactivité
Le rayonnement radioactif a plusieurs applications dans des domaines diverses :
- L'industrie : Production de l'énergie électrique, des semi-conducteurs, ...
- La médecine : Stériliser le matériel médical, traitement des cancers, ...
- L'agriculture : Prolonger la durée de conservation des produits, éviter les insectes nuisibles, ...
5.3 Dangers de la radioactivité
La production des bombes nucléaires (fusion nucléaire), et des bombes atomiques (fission nucléaire) de destruction massive (énorme). Elles produisent des rayonnements en quantités importantes qui tuent les être-vivants et rend l'environnement non vivable pendant une longue durée.